
อาเมเดโอ อาโวกาโดร(Lorenzo Romano Amedeo Carlo Avogadro ค.ศ.1776 - 1856)
นักวิทยาศาสตร์ชาวอิตาลีชื่อ อาเมเดโอ อาโวกาโดร ได้ศึกษาความสัมพันธ์ระหว่างปริมาตรกับปริมาณของแก๊ส โดยเขาได้เสนอสมมติฐานไว้ในปี ค.ศ. 1811 ว่า "ที่อุณหภูมิและความดันเดียวกัน แก๊สต่างชนิดกันที่มีปริมาตรเท่ากันจะมีจำนวนโมเลกุลเท่ากัน" ซึ่งหมายความว่า แก๊สทุกชนิดจะมีปริมาตรเพิ่มขึ้นเรื่อยๆ เมื่อจำนวนโมเลกุลของแก๊สเพิ่มขึ้นเรื่อยๆ เช่นกัน แต่ข้อสมมติฐานของเขาไม่ได้รับการยอมรับจากวงการวิทยาศาสตร์ในสมัยนั้นเป็นเวลาเกือบ 50 ปี และต่อมาเมื่อ สตานิซาโล คานนิซาโร(Stanisalo Cannizaro) ได้ทดลองพิสูจน์และได้นำเสนอในที่ประชุมวิทยาศาสตร์เมื่อปี ค.ศ. 1860 สมมติฐานของอาโวกาโดรจึงได้รับการยอมรับในที่สุด และเพื่อเป็นเกียรติแก่อาโวการโดร ตัวเลข 1 โมลซึ่งเท่ากับ 6.02 x 1023 จึงเรียกว่า เลขอาโวกาโดร (Avogadro Number) จากข้อสมมติฐานของอาโวกาโดรเมื่อได้ทดลองซ้ำต่อมาหลายๆ ครั้งก็ยืนยันความสัมพันธ์ที่เป็นไปตามสมมติฐานอาโวกาโดร จึงตั้งเป็นกฏของอาโวกาโดรขึ้นมา ซึ่งกล่าวว่า "ที่ความดันและอุณหภูมิของแก๊สคงที่ ปริมาตรของแก๊สจะแปรผันตรงกับจำนวนโมเลกุลหรือจำนวนโมลของแก๊สนั้น" ดังแผนภาพด้านล่าง
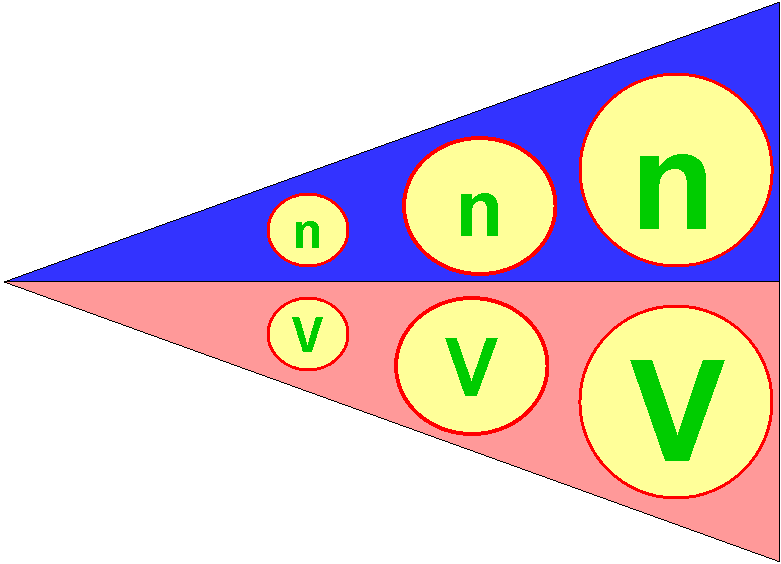
เมื่อ n คือจำนวนโมล และ V คือปริมาตรของแก๊ส
จากแผนภาพ เมื่อ n มีจำนวนน้อย V ก็จะน้อยด้วย แต่เมื่อ n มีจำนวนมากขึ้น V ก็จะมากขึ้นตามไปด้วย จากสมมติฐานของอาโวกาโดรเขียนเป็นความสัมพันธ์ทางคณิตศาสตร์ได้ว่า ปริมาตรของแก๊ส แปรผันตรงกับจำนวนโมลของแก๊ส
เมื่อ k เป็นค่าคงที่ของการแปรผัน
อัตราส่วนของปริมาตรกับจำนวนโมลของแก๊สจะเป็นค่าคงที่ k
ที่ สภาวะ STP แก๊สทุกชนิด 1 โมล มีปริมาตรเท่ากับ 22.4 L
